اصل لوشاتولیه
اصل لوشاتولیه در واقع بیانی از قانون سوم نیوتون است. وقتی سیستمی در حال تعادل در معرض تغییر شرایط قرار میگیرد، خود را چنان تنظیم میکند تا با آن تغییر کند. این اصل نتیجه قانون بقای (پایستگی) انرژی است.
بنابراصل لوشاتولیه، چنانچه سامانهای در حال تعادل باشد، در برابر هرگونه تغییری در جهت مخالف واکنش نشان میدهد تا اثر آن را از بین ببرد.
اصل لوشاتلیه سامانههای با تغییرات غیر آنی را بررسی میکند؛ و مدت زمان پایدار شدن سامانه بستگی به شدت بازخورد منفی نسبت به شوک مکانیکی اولیه دارد.
هنگامی که یک شوک بازخورد مثبتی را در سامانه ایجاد میکند، تعادل جدیدی که در سامانه برقرار خواهد شد ممکن است تفاوت زیادی با وضعیت تعادل اولیه داشته باشد، یا مدت زمان رسیدن به آن زیاد باشد. در برخی سامانههای پویا وضعیت پایانی را نمیتوان از روی شوک تعیین کرد. این اصل برای بررسی سامانههای بازخورد منفی بسته به کار میرود اما بهطور کلی در طبیعت برقرار است.
جورج گاموف در سال ۱۹۶۳ گفت: با کمی تأمل میتوان گفت که اگر قرار است بقای انرژی داشته باشیم این اصل لزوماً صحت دارد، وگرنه ماشینهای حرکت دائم چیزهایی به ارزش ده سنت بودند و ما میتوانستیم مقدار زیادی انرژی با کمی کار تولید کنیم.
ماشینهای حرکت دائم هنوز هم افرادی را افسون میکند و اگر این واژهها را در اینترنت جستجو کنید، هزاران جایگاه بر روز صفحه نمایشگر کامپیوتر همواره شما را سرگرم خواهد کرد.
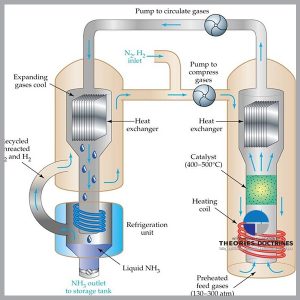
کاربرد اصل لوشاتولیه در شیمی
اصل لوشاتولیه در فهم روش کنترل تولید صنعتی مواد شیمیایی مانند آمونیاک بسیار گرانبهاست.
در تولید آمونیاک نیتروژن و هیدروژن با همدیگر ترکیب میشوند آمونیاک به وجود میآورند؛ یعنی، نیتروژن + هیدروژن ↔آمونیاک (دو پیکان نشان میدهد که واکنش دو طرفی است.) وقتی فشار این سیستم افزایش مییابد آمونیاک بیشتری تولید میشود.
اما وقتی فشار کاهش مییابد آمونیاک به نیتروژن و هیدروژن تجزیه میشود. به این ترتیب، شیمیدانها با کنترل فشار و دما میتوانند آمونیاک را با کمترین ضایعات تولید کنند.
لوشاتولیه شیمیدان بود و در دانشکده معادن پاریس تدریس میکرد. او به خاطر اختراع ترموکوپل برای اندازه گیری دماهای بالا (۱۸۷۷) و جوشکاری استیلن (۱۸۹۵) نیز معروف است.










دیدگاهتان را بنویسید